(来源:武汉大学新闻网)近日,武汉大学公共卫生学院缪小平/田剑波教授团队与商汤科技研究院张少霆团队合作,在Nature子刊Nature Communications(IF: 16)在线发表了题为Genome-wide association analysis of left ventricular imaging-derived phenotypes identifies 72 risk loci and yields genetic insights into hypertrophic cardiomyopathy的研究论文。

左心室结构和功能的变化与多种心血管疾病(cardiovascular diseases,CVDs)如高血压、房颤、心肌病和心力衰竭等密切相关。目前,通过大规模心脏磁共振(Cardiovascular magnetic resonance, CMR)成像数据进行全基因组关联研究(GWAS)已经揭示了与心脏体积相关指标(如左室收缩末期容积(LVESV)、左心室射血分数(LVEF)和每搏输出量(SV)等)相关的多个遗传位点,但这些指标并不能充分解释这些心血管疾病的发生。一些研究提示,左心室室壁区域厚度(Left ventricular regional wall thickness,LVRWT)在心肌病、舒张功能障碍和心室心律失常等心脏疾病中起到了独立预测的作用,因此对LVRWT的遗传结构进行识别和解析具有重要的公共卫生意义。另一方面,由于不同受试者心脏结构的高度可变性,目前临床经验丰富的影像医生数量远远满足不了对心脏壁厚度识别准确估计需求。因此,迫切需求开展对LVRWT成像表型进行大规模无偏倚图像识别和遗传结构解析等相关研究。
为解决上述问题,研究者首次开发了一种名为心肌分割测量方法(Myocardial Segmentation and Measurement Method, MSMM)的深度学习计算框架。该方法通过对CMR图像进行人工智能高通量识别,能够快速而准确地定量LVRWT,且相比目前常用的图像识别算法,在识别速度和准确性方面表现出一定的优势。该方法系统定量出12个LVRWT指标,分别对应收缩末期和舒张末期的不同心室壁区域,为研究提供了更详尽的心脏结构信息。接着,研究者将MSMM方法应用于超过45000名具有CMR图像和遗传数据的人群,对这些LVRWT指标进行了细致的遗传分析。
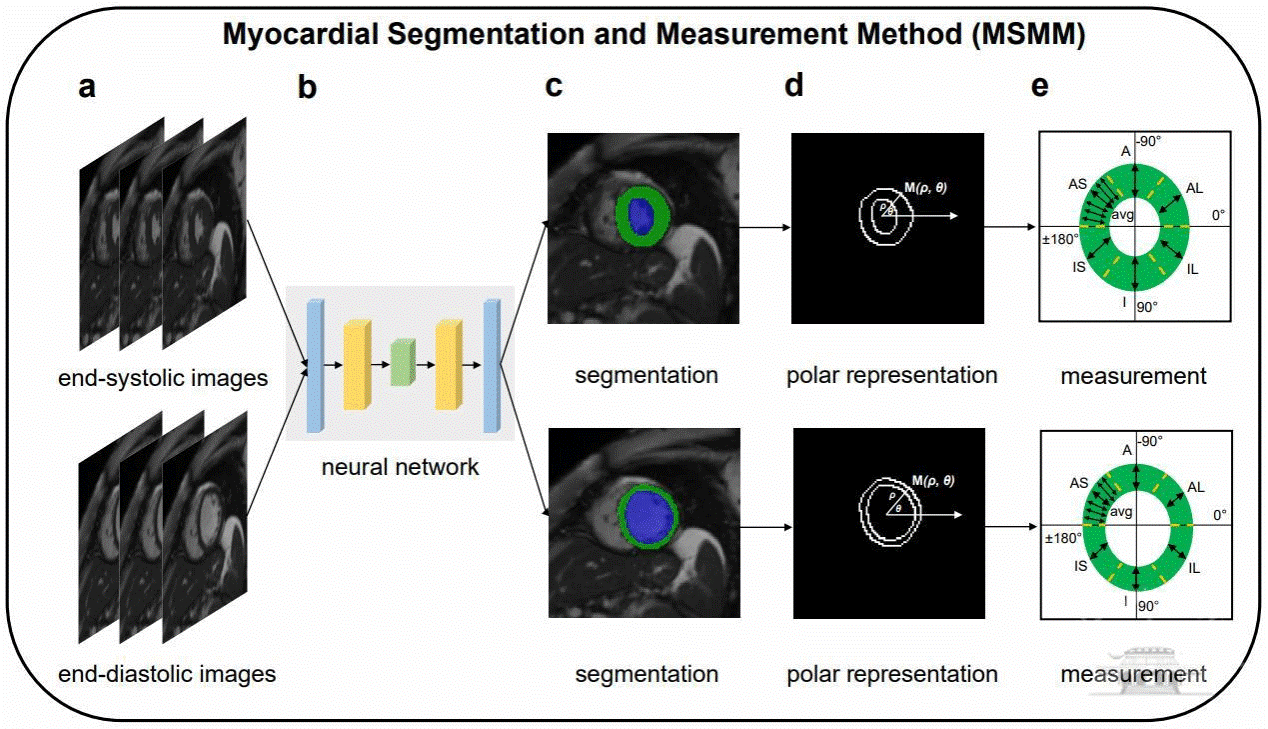
随后,研究者对上述12个LVRWTs指标进行系统遗传易感位点分析, 共发现72个显著的遗传位点(P <5×10−8),这些位点高度富集在CVDs相关的风险区域,特别是肥厚性心肌病(hypertrophic cardiomyopathy, HCM)。接着研究者通过遗传精细定位,在收缩末期和舒张末期分别鉴定了127个和95个候选基因,包括ALPK3、HCM、SYNPO2L等,这些基因主要参与心脏发育和收缩,以及Z盘通路激活等过程。这些结果表明LVRWTs相关的遗传位点可能在心肌病的发展中发挥重要作用。进一步,研究者将这12个LVRWTs与11种高发的CVDs进行遗传相关性和孟德尔随机化因果推断分析,发现LVRWTs与多种CVDs存在着遗传关联,特别是与HCM之间存在显著的因果关系(P< 0.01)。最后,研究者建立了每个LVRWT性状的多基因风险评分(polygenic risk score, PRS),并在439,981名未接受CMR检查的队列中验证LVRWT-PRS是否具有识别HCM的能力。结果发现,特别是收缩末期室间隔中部来源的PRS也能够较好地预测HCM发病风险(HR = 1.69, 95%CI = 1.33-2.15,P = 2.31×10−5)。
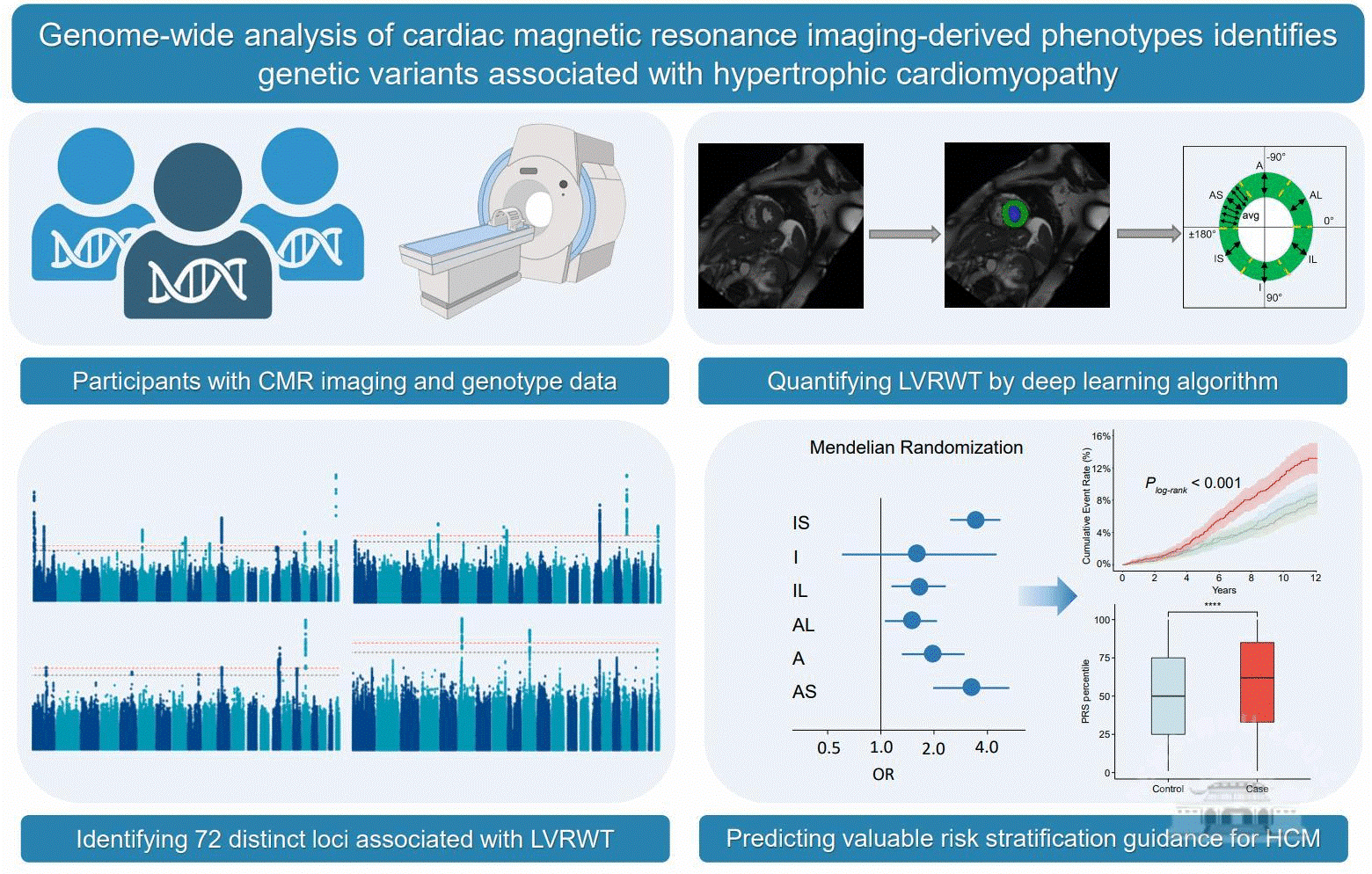
综上所述,该研究结合人工智能图像识别算法和遗传结构分析系统解析了左心室室壁厚度的遗传结构,为解析左心室结构和功能提供了重要的补充信息,同时也为理解相关CVDs的发生提供了新的方向,特别是所开发的PRS在无法进行CMR检查的人群中具有极大的临床应用潜力,能够及早发现HCM高危人群个体。